晚期實體瘤的CAR-T細胞療法臨床實驗數(shù)據(jù)喜人
AACR 2019年會上呈現(xiàn)的一組研究顯示��,對晚期實體瘤病人采用兩種不同的CAR T細胞療法�,得到了喜人的臨床效果�。
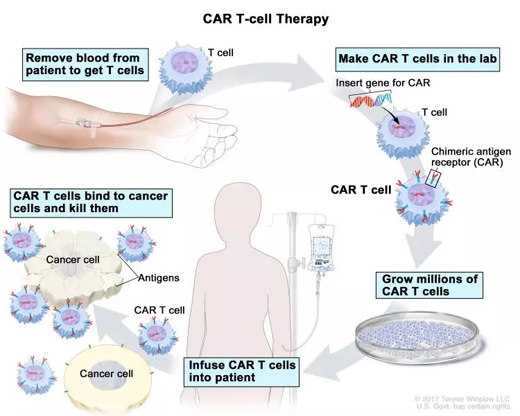
CAR T細胞療法是一種免疫療法,其中把T細胞從病人體內(nèi)提取�,進行基因修改,使得它們可以識別病人的癌細胞�����。修改后的T細胞重新進入病人體內(nèi)后�����,數(shù)量激增�����,攻擊癌細胞�。美國FDA已批準兩種CAR T細胞療法,用于血癌的治療:Tisagenlecleucel (Kymriah) 用于治療急性淋巴細胞白血病和非霍奇金淋巴瘤者�����。axicabtagene ciloleucel (Yescarta) 用于非霍奇金淋巴瘤的成年患者�����。
CAR T細胞在血癌的治療領(lǐng)域里獲得了成功��,那么接下來讓人期待的發(fā)展就是該療法今后可用于實體瘤的治療。CAR T細胞療法用于實體瘤的治療是具挑戰(zhàn)性的���,研究人員在這方面也有過幾次失敗的嘗試經(jīng)歷����。遇到的挑戰(zhàn)包括怎么為T細胞找到正確的靶向�,T細胞如何在一個常免疫抑制微環(huán)境激增��,怎樣產(chǎn)生有效的抗腫瘤響應(yīng)���,以及怎樣避免嚴重的副作用��。的評論文章總結(jié)了CAR T細胞療法用于實體瘤治療的挑戰(zhàn)和攻克策略�。也列舉了一些進行中的臨床實驗中���,靶向腫瘤抗原(包括GD2�、CEA和EGFR)的CAR T細胞試驗于多種實體瘤����。會議中展示的數(shù)據(jù)表明,發(fā)展CAR T細胞療法來治療實體瘤��,不僅僅是安全的,并且�,病人可獲得臨床益處。
靶向間皮素CAR T細胞療法治療惡性胸膜疾病
在一個一期臨床實驗中�,來自于紀念斯隆凱特琳癌癥中心的研究人員做了實驗,判定他們研發(fā)的靶向間皮素CAR T細胞對于間皮瘤����、肺癌和乳腺癌引起的惡性胸膜疾病病人是否安全而有效。
研究小組研發(fā)了名為IcasM28z的CAR T細胞��,靶向細胞表面蛋白�,即間皮素,間皮素在大部分癌細胞上表達�。小組設(shè)法用區(qū)域傳送技術(shù)把CAR T細胞直接送達腫瘤位置。Prasad S. Adusumilli博士��,即該研究的發(fā)表人表示:“如果該方法成功���,美國每年200萬名間皮素表達的實體瘤病人將從中獲益”��。Cancer Discovery發(fā)布了這一文章��,文章回顧了表達間皮素的實體瘤種類���,還展望了靶向間皮素CAR T細胞療法用于此類惡性腫瘤的治療潛力���。
因為體內(nèi)的一些正常細胞表達低水平的間皮素,所以靶向間皮素CAR T細胞可對它們產(chǎn)生毒性���。為此�����,研究小組,包括高級作者Michel Sadelain博士����,加入了保證安全的“自殺”開關(guān),即Icaspase-9(inducible caspase-9)��,病人萬一遇到無法預(yù)測的毒性情況下����,它可自動開啟,所有CAR T細胞全部被清除干凈�。然而,實驗中�,在實驗劑量下,研究者未檢測到任何嚴重毒性��。
利用介入放射療法,研究人員向21名惡性胸膜疾病患者(19名患有惡性胸膜間皮瘤�,一名患有轉(zhuǎn)移性肺癌,另一名患有轉(zhuǎn)移性乳腺癌)的胸膜腔直接注入IcasM28z CAR T細胞����。
在為期38周的評估期內(nèi),在13名患者體內(nèi)��,觀察到IcasM28z CAR T細胞在周邊血液內(nèi)持久而穩(wěn)定�,而病人血清間皮素相關(guān)蛋白水平下降50%、影像學研究下發(fā)現(xiàn)腫瘤衰退現(xiàn)象��。這兩者之間存在聯(lián)系�。
其中一位間皮瘤病人接受了治愈性手術(shù)和胸部放療。在臨床前實驗里�,研究人員發(fā)現(xiàn)在大的腫瘤內(nèi),CAR T細胞趨于功能耗竭狀態(tài)�����。Anti-PD-1制劑療法可重新激活耗竭的CAR T細胞���,并清除一部分小鼠體內(nèi)的腫瘤���?�;谶@一原理�����,14名病人繼續(xù)接受了anti-PD1檢查點阻斷制劑���。21個周期的治療后,兩名病人分別在60周和32周時�,在PET掃描上呈現(xiàn)完整的代謝反應(yīng)。并且這種代謝反應(yīng)在本報告編寫時仍持續(xù)���;五名病人呈部分反應(yīng),而四名病人病情穩(wěn)定�����。
Adusumilli在一篇新聞發(fā)表中提到:“結(jié)合合理研發(fā)的策略����,如介入放療、T細胞基因工程和的免疫制劑��,可獲得良好的療效,并為這一方法今后在進展性���、治療抵抗性癌癥(如間皮瘤)的治療奠定基礎(chǔ)��,這類癌癥��,用目前的療法都難以獲得較好的療效”�����。
靶向HER2 CAR T 細胞療法治療晚期肉瘤
針對復(fù)發(fā)性或治療抵抗性肉瘤患兒和成年患者的療法目前很有限�。有些肉瘤可通過治愈性挽救化療來治療��,但成功率很低�,且這些療法毒性很強。在一個一期臨床實驗中���,Shoba Navai博士(美國貝勒醫(yī)學院細胞和基因療法中心���、德州兒童醫(yī)院和休斯敦衛(wèi)理公會醫(yī)院)研究了靶向HER2 CAR T細胞和淋巴細胞刪除化療的結(jié)合療法在晚期HER2陽性肉瘤病人體內(nèi)的安全性。
Navai告訴我們����,腫瘤表面表達HER2的肉瘤比例并不確切�����,不過常見的骨肉瘤�,據(jù)報道其HER2陽性率高達40%��,而HER2陽性與高腫瘤轉(zhuǎn)移率有關(guān)���。然而����,靶向HER2的抗體��,如trastuzumab����,并未在臨床研究中表現(xiàn)出有效性。
Navai表示:“我們小組此前通過實驗室研究發(fā)現(xiàn)���,靶向HER2的CAR T細胞比trastuzumab更能有效靶向腫瘤細胞的低水平HER2,所以這些CAR T細胞可能在肉瘤病人體內(nèi)有著更好的抗腫瘤效果��,可能是HER2抗體療法無法達到的效果”�。
Navai和同事���,包括研究者Meenakshi Hegde博士,對10名病人在淋巴細胞刪除(用氟達拉濱或氟達拉濱和環(huán)磷酰胺)后進行總共三次靶向HER2 CAR T細胞輸注����。病人年齡在4-54歲之間,患有難治性/轉(zhuǎn)移性HER2陽性肉瘤(5名骨肉瘤患者�、3名橫紋肌肉瘤,一名尤文肉瘤����,一名滑膜肉瘤)。他們此前已接受過五次挽救治療���。
對初始靶向HER2 CAR T細胞療法有響應(yīng)的病人會再接受五次CAR T細胞輸注(不作淋巴細胞刪除)���。在所有病人體內(nèi)都發(fā)現(xiàn)了CAR T的激增,其中兩名病人的激增峰值中位數(shù)出現(xiàn)在第7天�。輸注后6周時,CAR T細胞在所有病人體內(nèi)被檢測到�。
一名骨肉瘤轉(zhuǎn)移至肺部的患兒連續(xù)32個月對CART細胞有持續(xù)響應(yīng)。三名病人病情穩(wěn)定���,五名病人病情進展�����。另一名橫紋肌肉瘤轉(zhuǎn)移至骨髓的患兒連續(xù)12個月產(chǎn)生完全響應(yīng)�����,但之后復(fù)發(fā)�;應(yīng)用CAR T細胞療法后,已連續(xù)17個月產(chǎn)生完全響應(yīng)�����。通過在不同時間點對該病人血清進行蛋白質(zhì)組分析后發(fā)現(xiàn)了對細胞內(nèi)蛋白的抗體抵抗(細胞內(nèi)蛋白存在于細胞周期���、細胞成長和細胞信號傳導和腫瘤進展�����,如腫瘤侵襲和轉(zhuǎn)移)����。
Navai表示:“該病人血液中的某些抗體是新測得的�,并且在CAR T細胞輸注后維持��。表明除了我們預(yù)測到的CAR T靶向HER2后的直接療效之外,這一療法很可能激活了病人自身的免疫系統(tǒng)”�。
Navai告訴我們,總體來說����,這一實驗中的病人受到的治療相關(guān)毒性有限。大部分病人在輸注了CAR T細胞后的24小時內(nèi)發(fā)燒���,但都獲得了及時進行護理��,三天內(nèi)退熱�����。所有病人在化療后出現(xiàn)了預(yù)期中的血細胞計數(shù)降低���,隨后恢復(fù)正常;沒有發(fā)現(xiàn)因低血細胞計數(shù)引起的繼發(fā)感染情況���。沒有發(fā)現(xiàn)心功能降低或肺毒性�����。
Navai表示:“我們的研究表明�����,靶向HER2的CAR T細胞療法結(jié)合淋巴細胞刪除化療�,是很安全的。盡管�,還有很長的路要走,但在一些晚期HER2陽性肉瘤病人中已顯現(xiàn)出十分喜人的抗腫瘤潛力”�。
聲明:本文版權(quán)歸原作者所有,轉(zhuǎn)載文章僅為傳播更多信息�����,如作者信息標記有誤�����,或侵犯您的版權(quán)���,請聯(lián)系我們���,我們將在及時修改或刪除內(nèi)容,聯(lián)系郵箱:marketing@360worldcare.com
