日前����,Aprea Therapeutics公司宣布�,美國FDA授予其在研療法APR-246突破性療法認(rèn)定�����,與azacitidine聯(lián)用����,治療攜帶TP53基因突變的骨髓增生異常綜合征(MDS)患者�。

MDS是一種因骨髓中血細(xì)胞的成熟缺陷,導(dǎo)致不能產(chǎn)生足夠健康血細(xì)胞的癌癥�,它的癥狀包括嚴(yán)重甚至致命的貧血。大約30%至40%的MDS患者會(huì)進(jìn)展為急性髓系白血?��。ˋML)�����。
p53是在腫瘤病毒研究的優(yōu)異時(shí)期被發(fā)現(xiàn)的�,初它被認(rèn)為是致癌蛋白�����,但是隨后的研究發(fā)現(xiàn)野生型(wild type)p53在細(xì)胞培養(yǎng)環(huán)境下抑制腫瘤生長和細(xì)胞癌變�。編碼p53的TP53基因中出現(xiàn)的失活性突變?cè)谌祟惸[瘤中非常常見。在很多癌癥中�����,TP53基因突變與患者的不良預(yù)后相關(guān),通常與抗癌藥的耐藥性和較差的總體生存率也相關(guān)�����。目前����,沒有針對(duì)這一MDS患者群體的治療選擇出現(xiàn)�。
APR-246是一款小分子藥物,可“重新激活”已經(jīng)突變失活的p53蛋白�����。它已在許多治療實(shí)體腫瘤和血液癌癥的臨床前研究中觀察到抗腫瘤活性��,包括MDS���,AML和卵巢癌��。此外���,它還在與傳統(tǒng)抗癌療法(如化療),新型抗癌藥����,和免疫腫瘤檢查點(diǎn)抑制劑的聯(lián)合治療中展現(xiàn)了強(qiáng)大的協(xié)同作用�����。Aprea公司在1/2期臨床研究中��,證明了APR-246良好的安全性�����,以及對(duì)惡性血液腫瘤和攜帶TP53基因突變實(shí)體瘤的臨床緩解��。APR-246和azacitidine聯(lián)合�����,作為一線療法治療攜帶TP53突變MDS患者的關(guān)鍵性3期臨床研究正在進(jìn)行中�����。此前�,APlR-246已獲得FDA授予治療MDS患者的孤兒藥資格和快速通道資格�,以及歐洲藥品管理局(EMA)授予治療MDS,AML和卵巢癌患者的孤兒藥資格���。
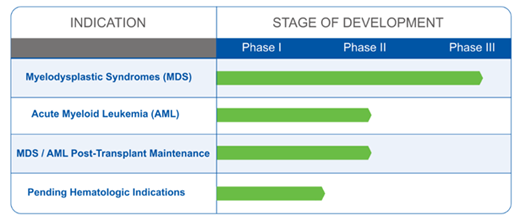
▲APR-246的研發(fā)管線(圖片來源:Aprea官網(wǎng))
“該突破性療法認(rèn)定進(jìn)一步支持了APR-246與azacitidine聯(lián)合治療攜帶TP53突變MDS患者的開發(fā)計(jì)劃�,”Aprea執(zhí)行官Christian S. Schade先生說:“攜帶TP53突變的MDS患者的預(yù)后很差,而且目前沒有針對(duì)這些患者的治療選擇出現(xiàn)����。我們希望可以與FDA繼續(xù)合作,進(jìn)一步推進(jìn)APR-246的臨床開發(fā)計(jì)劃�?����!?/span>
參考資料:
[1] Aprea Therapeutics Receives FDA Breakthrough Therapy Designation for APR-246 in Combination with Azacitidine for the Treatment of Myelodysplastic Syndromes (MDS) with a TP53 Mutation����,Retrieved January 30, 2020, from https://ir.aprea.com/news-releases/news-release-details/aprea-therapeutics-receives-fda-breakthrough-therapy-designation
聲明:本文版權(quán)歸原作者所有,轉(zhuǎn)載文章僅為傳播更多信息�,如作者信息標(biāo)記有誤,或侵犯您的版權(quán)�,請(qǐng)聯(lián)系我們,我們將在及時(shí)修改或刪除內(nèi)容�,聯(lián)系郵箱:marketing@360worldcare.com

